初のHIV感染予防薬、承認を勧告 米FDA諮問委
このニュースをシェア
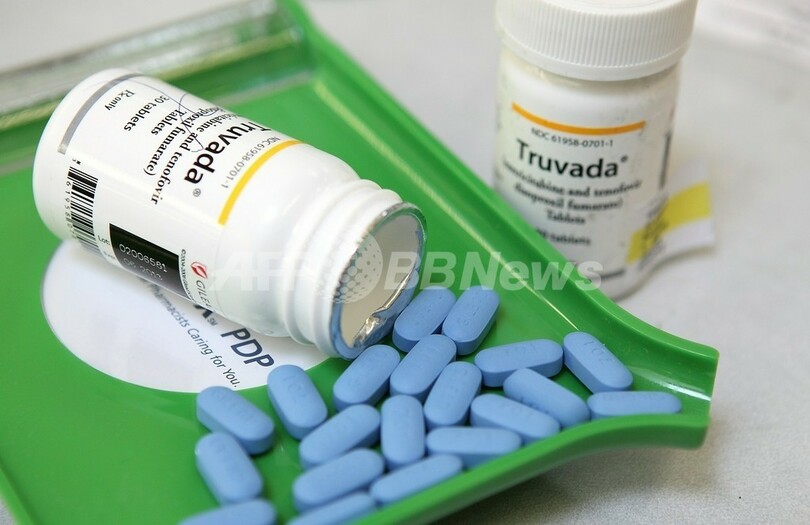
【5月11日 AFP】米食品医薬品局(Food and Drug Administration、FDA)の諮問委員会は10日、現在HIV/AIDS患者の治療に使用されている抗レトロウイルス薬「ツルバダ(Truvada)」について、史上初のHIV感染予防薬として承認するよう勧告した。
米製薬会社ギリアド・サイエンシズ(Gilead Sciences)が開発したツルバダは、他の抗HIV薬と併用するHIV/AIDS治療薬として2004年に承認を受けている。しかし2010年に行われた臨床試験では、HIV感染リスクが高い男性同性愛者などに同薬を服用してもらったところ、定期的に服用した被験者で最大約73%感染が予防できるとの結果が出ていた。
11時間に及んだFDAのエイズワクチン諮問委員会(AIDS Vaccine Advocacy Coalition、AVAC)の協議では、ツルバダを予防薬と認定することで感染リスクの高い性行為が増える可能性や、耐性ウイルスが生じる懸念が30人余りの有識者から指摘されたが、最終的にはツルバダをHIV感染予防薬として承認すべきとの結論に達した。
FDAは諮問委の勧告に従う義務はないが、勧告どおり承認するのが通例となっている。FDAによる最終決定は6月中旬に出される予定。(c)AFP/Kerry Sheridan
【関連記事】
・「エイズの最終的な克服に希望」、米感染症研究所長
・エイズワクチン、いよいよ実現へ 開発の第一人者に聞く
・サイエンス誌の科学10大成果、1位はHIV治療薬の効果
米製薬会社ギリアド・サイエンシズ(Gilead Sciences)が開発したツルバダは、他の抗HIV薬と併用するHIV/AIDS治療薬として2004年に承認を受けている。しかし2010年に行われた臨床試験では、HIV感染リスクが高い男性同性愛者などに同薬を服用してもらったところ、定期的に服用した被験者で最大約73%感染が予防できるとの結果が出ていた。
11時間に及んだFDAのエイズワクチン諮問委員会(AIDS Vaccine Advocacy Coalition、AVAC)の協議では、ツルバダを予防薬と認定することで感染リスクの高い性行為が増える可能性や、耐性ウイルスが生じる懸念が30人余りの有識者から指摘されたが、最終的にはツルバダをHIV感染予防薬として承認すべきとの結論に達した。
FDAは諮問委の勧告に従う義務はないが、勧告どおり承認するのが通例となっている。FDAによる最終決定は6月中旬に出される予定。(c)AFP/Kerry Sheridan
【関連記事】
・「エイズの最終的な克服に希望」、米感染症研究所長
・エイズワクチン、いよいよ実現へ 開発の第一人者に聞く
・サイエンス誌の科学10大成果、1位はHIV治療薬の効果






